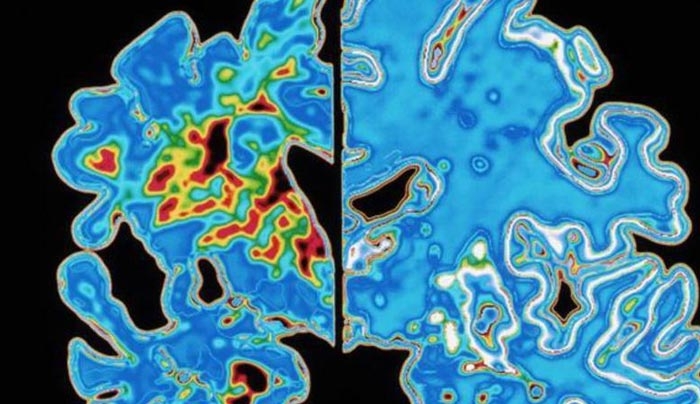
Η πρωτεΐνη PGC-1-alpha, που κωδικοποιείται από το συγκεκριμένο γονίδιο, εμποδίζει να σχηματισθούν οι καταστροφικές πλάκες αμυλοειδούς στον εγκέφαλο.
Αν και η σχετική έρευνα, που χρηματοδοτείται από το Ευρωπαϊκό Συμβούλιο Έρευνας (ERC) και από τoν βρετανικό ερευνητικό φορέα Alzheimer's Research UK, βρίσκεται ακόμη στο αρχικό στάδιο, ανοίγει νέους δρόμους για την αντιμετώπιση της συνεχώς εξαπλούμενης νευροεκφυλιστικής πάθησης.
Παγκοσμίως περίπου 47,5 εκατομμύρια άνθρωποι πάσχουν από άνοια, με κυριότερη αιτία τη νόσο Αλτσχάιμερ (πάνω από 40 εκατ. ασθενείς), για την οποία μέχρι στιγμής δεν υπάρχει θεραπεία. Τα υπάρχοντα φάρμακα δεν αντιμετωπίζουν τις υποκείμενες αιτίες, αλλά απλώς αντιμετωπίζουν ορισμένα συμπτώματα ή επιβραδύνουν κάπως την εξέλιξη της νόσου.
Οι ερευνητές, με επικεφαλής τον καθηγητή Νικόλα Μαζαράκη και τη δρα Μαγκνταλένα Σάστρε της Ιατρικής Σχολής του Imperial College του Λονδίνου, έκαναν τη σχετική δημοσίευση στο περιοδικό της Εθνικής Ακαδημίας Επιστημών των ΗΠΑ (PNAS). Στην έρευνα συμμετείχαν επίσης η Λουκία Κατσούρη (πρώτη συγγραφέας της μελέτης) και η Ιωάννα Ελευθεριάδου.
Προηγούμενες μελέτες της ίδιας ερευνητικής ομάδας σε κυτταρικές καλλιέργειες στο εργαστήριο είχαν δείξει ότι το εν λόγω γονίδιο PGC-1-alpha μπορεί να εμποδίσει τον σχηματισμό των χαρακτηριστικών πλακών από την πρωτεΐνη βήτα αμυλοειδές, οι οποίες εμφανίζονται στον εγκέφαλο των ασθενών με Αλτσχάιμερ και οδηγούν σε καταστροφή των εγκεφαλικών κυττάρων.
 |
Αυτή τη φορά το γονίδιο εισήχθη στον εγκέφαλο πειραματόζωων, με «όχημα» έναν τροποποιημένο αβλαβή ιό. Οι επιστήμονες στόχευσαν το γονίδιο στον ιππόκαμπο και στον φλοιό, δηλαδή στις πρώτες περιοχές του εγκεφάλου όπου αναπτύσσονται οι πλάκες του αμυλοειδούς στους ασθενείς με Αλτσχάιμερ.
Οι βλάβες στον ιππόκαμπο οδηγούν σε απώλεια της μνήμης για τα πρόσφατα γεγονότα, καθώς και σε απώλεια προσανατολισμού στο χώρο, ενώ οι βλάβες στον εγκεφαλικό φλοιό έχουν ευρύτερες επιπτώσεις στην μακρόχρονη μνήμη, στη λογική, στη σκέψη και στην ψυχική διάθεση.
Η εισαγωγή του γονιδίου PGC-1-alpha στα ποντίκια έγινε με ένεση στον εγκέφαλο, όταν η νόσος βρισκόταν ακόμη στα αρχικά στάδια. Μετά από τέσσερις μήνες, τα ποντίκια που είχαν κάνει τη γονιδιακή θεραπεία, είχαν πολύ λίγες πλάκες αμυλοειδούς, σε σύγκριση με τα τρωκτικά όπου δεν είχε εισαχθεί το εν λόγω γονίδιο και τα οποία είχαν πλέον πολλές τέτοιες πλάκες.
Επιπλέον, τα ποντίκια με το γονίδιο τα πήγαν εξίσου καλά στα τεστ μνήμης με τα υγιή ποντίκια. Ακόμη, τα πειραματόζωα που είχαν δεχθεί το γονίδιο, δεν εμφάνιζαν καμία απώλεια εγκεφαλικών κυττάρων στον ιππόκαμπό τους.
Η πρωτεΐνη PGC-1-alpha που κωδικοποιείται από το ομώνυμο γονίδιο, εμπλέκεται στις μεταβολικές διαδικασίες του σώματος, μεταξύ άλλων στη ρύθμιση του σακχάρου και στον μεταβολισμό των λιπών. Προηγούμενες μελέτες έχουν δείξει ότι τόσο η σωματική άσκηση, όσο και η ουσία ρεσβερατρόλη που υπάρχει στο κόκκινο κρασί (αλλά μόνο σε μορφή χαπιού, επειδή το αλκοόλ ακυρώνει τα οφέλη της), μπορούν να αυξήσουν τα επίπεδα της συγκεκριμένης πρωτεΐνης στον οργανισμό.
Το επόμενο βήμα, κατά τους ερευνητές, θα είναι να προχωρήσουν πλέον σε δοκιμές σε ανθρώπους, με την ελπίδα ότι το γονίδιο θα είναι κατ' εξοχήν ωφέλιμο στα αρχικά στάδια της νόσου, όταν εμφανίζονται τα πρώτα συμπτώματα. Αν και μια πιθανή κλινική χρήση της νέας θεραπείας απέχει ακόμη χρόνια, εωσότου επιβεβαιωθεί ότι είναι ασφαλής και αποτελεσματική σε ασθενείς, τα έως τώρα ευρήματα γεννούν μια συγκρατημένη αισιοδοξία.
Συνέντευξη του καθηγητή Ν.Μαζαράκη στο ΑΠΕ-ΜΠΕ
Ο Νικόλας Μαζαράκης (γεν. 1961) σπούδασε βιολογία στο Πανεπιστήμιο του Ανατολικού Λονδίνου (1981-85) και πήρε το διδακτορικό του στη βιοχημεία και μοριακή γενετική από το Βασιλικό Κολλέγιο (King's College) του Πανεπιστημίου του Λονδίνου το 1989. Από το 2006 μέχρι σήμερα είναι καθηγητής μοριακής βιοϊατρικής και επικεφαλής του τομέα γονιδιακής θεραπείας στο Τμήμα Επιστημών του Εγκεφάλου της Ιατρικής Σχολής του Imperial College του Λονδίνου. Από το 2011 έχει εκλεγεί εταίρος της Βασιλικής Εταιρείας Βιολογίας της Βρετανίας.
Είναι ένας μοριακός νευροεπιστήμονας με διεθνή φήμη στη γενετική θεραπεία των νευρολογικών παθήσεων, με έρευνες τόσο στο πανεπιστήμιο, όσο και στην εταιρεία Oxford BioMedica plc. Πριν από το Αλτσχάιμερ, δοκίμασε με επιτυχία μια ανάλογη γονιδιακή θεραπεία στην περίπτωση ασθενών με προχωρημένη νόσο Πάρκινσον. Ο ελληνικής καταγωγής επιστήμονας μίλησε το Αθηναϊκό και Μακεδονικό Πρακτορείο Ειδήσεων για τη σημασία και τις προοπτικές της υπό ανάπτυξη γονιδιακής θεραπείας για τη νόσο Αλτσχάιμερ.
Όπως λέει, έως σήμερα διεθνώς είναι η δεύτερη γονιδιακή θεραπεία που προβάλλει ως εναλλακτική λύση στα υπάρχοντα φάρμακα. Τονίζει ότι οι κλινικές δοκιμές σε ανθρώπους μπορεί να αρχίσουν σε τρία έως πέντε χρόνια, εφόσον υπάρξει η δέουσα χρηματοδοτική υποστήριξη, ενώ δεν αποκλείει ότι η ίδια γονιδιακή θεραπεία θα μπορούσε να αξιοποιηθεί και στην περίπτωση της νόσου Πάρκινσον.
Ακολουθεί η συνέντευξη:
ΕΡ: Ποια είναι η σημασία της νέας έρευνάς σας, σε σχέση με άλλες θεραπευτικές προσπάθειες που ήδη βρίσκονται σε εξέλιξη στο πεδίο της νόσου Αλτσχάιμερ;
ΑΠ: Η νόσος Αλτσχάιμερ είναι η πιο κοινή νευροεκφυλιστική διαταραχή, η οποία πλήττει πάνω από 45 εκατομμύρια ανθρώπους σε όλο τον κόσμο. Σήμερα δεν υπάρχουν θεραπείες που να θεραπεύουν ή να σταματούν την εξέλιξη της νόσου. Οι περισσότερες από τις υπάρχουσες θεραπείες εστιάζουν σε φάρμακα χορηγούμενα από το στόμα, τα οποία όμως δεν έχουν αποδειχθεί αποτελεσματικά.
Η έρευνά μας δείχνει ότι η γονιδιακή θεραπεία θα μπορούσε να αποτελέσει μια πραγματική εναλλακτική λύση στα φάρμακα από το στόμα, εφόσον εφαρμοσθεί στο αρχικό στάδιο της νόσου. Μέχρι τώρα, μόνο μια γονιδιακή θεραπεία, η οποία χρησιμοποιεί τον νευρωνικό αυξητικό παράγοντα, που χορηγείται μέσω αδενο-σχετιζόμενων ιών (AAV2), έχει δοκιμασθεί κλινικά γι' αυτή τη νόσο. Συνεπώς η δική μας προσέγγιση, που μεταφέρει το θεραπευτικό γονίδιο PGC1α με φορέα έναν ιό, αποτελεί μια νέα εναλλακτική λύση.
ΕΡ: Πότε εκτιμάτε ότι θα αρχίσουν οι πρώτες κλινικές δοκιμές της θεραπείας σας σε ανθρώπους ασθενείς;
ΑΠ: Αυτό μπορεί να γίνει σε σχετικά σύντομο χρονικό διάστημα, τριών έως πέντε ετών, εάν εξασφαλισθεί επαρκής υποστήριξη για ένα τέτοιο πρόγραμμα από συμβούλια ερευνών και εταιρείες. Θα χρειασθούν πάντως προηγουμένως περισσότερες μελέτες, προκειμένου να αξιολογηθεί η αποτελεσματικότητα της θεραπείας σε πειραματόζωα, μετά την εμφάνιση της νόσου σε αυτά.
ΕΡ: Οπότε πόσο αισιόδοξος είστε για τις προοπτικές της νέας θεραπείας, παίρνοντας υπόψη τις έως τώρα δοκιμές σας σε κύτταρα και ζώα;
ΑΠ: Είναι πολύ ενθαρρυντικά και σημαντικά τα βασικά ευρήματά μας ότι τα ζώα με παθολογία Αλτσχάιμερ, που θεραπεύθηκαν με PGC-1α, αναπτύσσουν λιγότερες πλάκες αμυλοειδούς στον εγκέφαλό τους, αποδίδουν στα τεστ μνήμης εξίσου καλά με τα υγιή ποντίκια και δεν εμφανίζουν απώλεια νευρώνων στις περιοχές εκείνες που κατεξοχήν πλήττει η νόσος.
Μολονότι οι μελλοντικές δοκιμές στα πειραματόζωα μπορεί να βελτιώσουν περαιτέρω αυτά τα ευρήματα, το πραγματικό τεστ αποτελεσματικότητας της θεραπείας θα είναι η εφαρμογή της σε ασθενείς σε αρχικό στάδιο Αλτσχάιμερ. Στο μεταξύ, η ύπαρξη περισσότερο ενθαρρυντικών δεδομένων από τις κλινικές δοκιμές της θεραπείας σε άλλες νευροεκφυλιστικές παθήσεις μπορεί να ανοίξει το δρόμο για μια ταχεία εφαρμογή της σε ανθρώπους ασθενείς.
ΕΡ: Τι γίνεται, αλήθεια, με την προηγούμενη γονιδιακή θεραπεία σας για τη νόσο Πάρκινσον; Ποια είναι τα έως τώρα αποτελέσματά της σε ασθενείς και κατά πόσο αφορά το ίδιο θεραπευτικό γονίδιο;
ΑΠ: Η γονιδιακή θεραπεία Prosavin®, που παράγει ντοπαμίνη στον εγκέφαλο, έχει εφαρμοσθεί σε 15 ασθενείς με προχωρημένη νόσο Πάρκινσον, σε μια κλινική δοκιμή με πολύ ενθαρρυντικά αποτελέσματα. Μια δεύτερη καθοριστική κλινική δοκιμή σχεδιάζεται για το επόμενο έτος, με τη χρήση ενός βελτιωμένου φορέα-ιού.
Αυτές οι δοκιμές δεν χρησιμοποιούν το PGC-1α, αλλά άλλα γονίδια που συνθέτουν το νευροδιαβιβαστή ντοπαμίνη, που είναι ανεπαρκής στα βασικά γάγγλια των ασθενών με προχωρημένη νόσο Πάρκινσον. Όμως ήδη υπάρχουν μελέτες που δίνουν ενδείξεις πως το PGC-1α θα μπορούσε να χρησιμοποιηθεί και για τη θεραπεία του Πάρκινσον, αν εισαχθεί νωρίς στον εγκέφαλο.
Καθώς η υπάρχουσα θεραπεία με λεβοντόπα σταθεροποιεί μεν τους ασθενείς αρχικού σταδίου με Πάρκινσον, αλλά δεν προστατεύει τα νεύρα τους, μια γονιδιακή θεραπεία για το Πάρκινσον θα πρέπει να περιμένει, εωσότου τελειοποιηθεί μια νέα γενιά ιών-φορέων, που θα στοχεύουν στον εγκέφαλο, αλλά δεν εφαρμόζονται απευθείας σε αυτόν.
ΕΡ: Τελικά, υπάρχει περίπτωση να ανακαλύψουμε ποτέ μια πραγματική θεραπεία για τις υποκείμενες αιτίες του Αλτσχάιμερ και όχι απλώς μια ανακούφιση των συμπτωμάτων;
ΑΠ: Τόσο οι προσεγγίσεις που εστιάζουν στα συμπτώματα, όσο και αυτές που μεταβάλλουν την πορεία της νόσου, εφόσον είναι ασφαλείς και αποτελεσματικές, είναι χρήσιμες παρεμβάσεις για μια ανίατη ασθένεια. Είμαι αισιόδοξος -γι' αυτό, άλλωστε, ασχολούμαι ακόμη με την ιατρική έρευνα μετά από 30 χρόνια!- ότι θα πετύχουμε τελικά να αναπτύξουμε πραγματικά αποτελεσματικές θεραπείες γι' αυτές τις παθήσεις.
πηγή: ΑΠΕ-ΜΠΕ